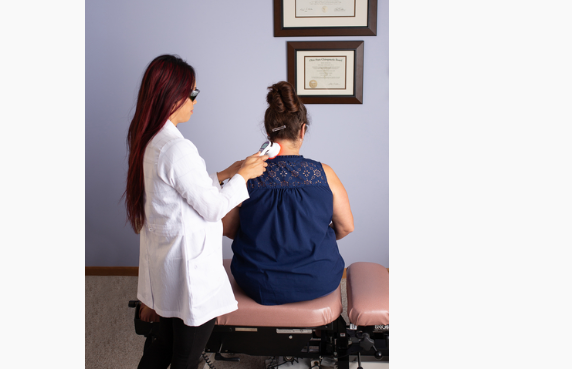
La terapia con láser FibroLux es una solución de vanguardia, no invasiva y sin medicamentos que proporciona un alivio rápido y eficaz mediante el uso de energía luminosa, en forma de fotones, para penetrar en las células, aumentando el flujo sanguíneo e interrumpiendo las señales del dolor. Clínicamente probado con efectos secundarios mínimos, FibroLux es un dispositivo portátil que apunta con precisión a 18 puntos de dolor, brindando alivio inmediato en solo 2 minutos por punto y un tiempo promedio de tratamiento de 6 a 10 minutos. (Foto: Business Wire)
SOLON, Ohio–( BUSINESS WIRE )–A la vanguardia de la tecnología de láser superpulsado, Multi Radiance Medical destaca el impacto del láser terapéutico FibroLux , uno de los primeros y únicos láseres terapéuticos aprobados por la FDA y diseñado para aliviar el dolor específicamente en personas que padecen Síndrome de fibromialgia. . Aprobado por la FDA en septiembre de 2022 y lanzado oficialmente a finales de 2023, FibroLux representa un paso importante para abordar los desafíos de la fibromialgia.
Se estima que la fibromialgia afecta a entre 5 y 8 millones de estadounidenses y se sabe que causa dolor y sensibilidad crónicos y generalizados, con opciones de tratamiento limitadas, a menudo acompañadas de efectos secundarios no deseados. El láser terapéutico FibroLux surge como una solución de vanguardia, no invasiva y libre de fármacos que proporciona un alivio rápido y eficaz mediante el uso de energía luminosa, en forma de fotones, para penetrar en las células, aumentando así la circulación sanguínea e interrumpiendo las señales cardíacas. Clínicamente probado con efectos secundarios mínimos, FibroLux es un dispositivo portátil que apunta con precisión a 18 puntos de dolor, brindando alivio inmediato en solo 2 minutos por punto y un tiempo promedio de tratamiento de 6 a 10 minutos.
“FibroLux, como uno de los primeros dispositivos médicos aprobados para la fibromialgia, representa un cambio de paradigma transformador, ya que proporciona un alivio que cambia la vida sin efectos secundarios”, dijo Max Kanarsky, presidente y director ejecutivo de Multi RadianceMedical. “Esta tecnología láser permite a las personas realizar sus actividades diarias sin la carga del dolor, brindando un rayo de esperanza a las personas discapacitadas por la fibromialgia. La reciente recepción positiva en conferencias médicas resalta la importancia de crear conciencia entre pacientes y médicos.
FibroLux mostró resultados notables en ensayos clínicos, con una reducción del 52 {f3a6a30fe8ec83c88e3a096004ddf2d5481b76e701b36185325949387956c891} en los puntos sensibles, una disminución del 53 {f3a6a30fe8ec83c88e3a096004ddf2d5481b76e701b36185325949387956c891} en el dolor y una mejora del 45 {f3a6a30fe8ec83c88e3a096004ddf2d5481b76e701b36185325949387956c891} en las puntuaciones del Cuestionario de Impacto de la Fibromialgia. En el innovador estudio revisado por pares , “La terapia de fotobiomodulación combinada con campo magnético estático es mejor que el placebo en pacientes con fibromialgia: un ensayo aleatorizado controlado con placebo”, el 86,67 {f3a6a30fe8ec83c88e3a096004ddf2d5481b76e701b36185325949387956c891} de los sujetos tratados con FibroLux cumplieron los criterios de éxito, muy por encima del 48,89 {f3a6a30fe8ec83c88e3a096004ddf2d5481b76e701b36185325949387956c891}. tasa de éxito en el grupo placebo.
FibroLux está a la vanguardia de la innovación en el tratamiento de la fibromialgia, mejorando la calidad de vida de las personas que padecen dolor crónico.Multi Radiance Medical se ha dedicado a promover soluciones médicas de vanguardia durante más de 15 años, y FibroLux ejemplifica su compromiso de brindar terapias efectivas, no invasivas y clínicamente probadas que permitan a las personas regresar a un estilo de vida activo y sin dolor. Desde sus inicios, la tecnología de MRM ha sido objeto de más de 59 artículos revisados por pares y la empresa ha participado activamente en más de 35 ensayos clínicos globales.
.